Aminoácidos ordinarios y síntesis de proteínas
Los aminoácidos que aparecen con mayor frecuencia en las estructuras proteicas de los organismos vivos se denominan aminoácidos ordinarios o proteinogénicos. Aunque en la naturaleza se conocen más de 500 tipos de aminoácidos, solo hay veinte a los que llamamos ordinarios. Junto con ellos, hay algunos más raros, llamados ocasional, que generalmente derivan del metabolismo de los ordinarios después de su incorporación a la cadena proteica. En el colágeno, por ejemplo, la lisina y la prolina, dos aminoácidos ordinarios, se encuentran en forma hidroxilada (hidroxiprolina e hidroxilisina).
La mayoría de los otros aminoácidos no ordinarios se encuentran principalmente dentro de la constitución de enzimas y hormonas de naturaleza proteica, o más bien péptidos (recuerde que para ser considerada tal, una proteína debe estar compuesta por más de 100 aminoácidos, mientras que para formar un oligo y un polipéptido 2 a 9 y 10 a 100 son suficientes).
Entre los 20 aminoácidos ordinarios se recuerdan
Alanina, Arginina, Asparagina, Acido aspartico, Cisteina, Glicina, Acido glutammico, Glutammina, Istidina, Isoleucina, Leucina, Lisina, Metionina, Fenilalanina, Prolina, Serina, Treonina, Triptofano, Tirosina, Valina
Ejemplos de aminoácidos no ordinarios son:
carnitina (involucrada en el transporte de ácidos grasos de cadena larga hacia la mitocondria, donde se utilizan para obtener energía);
ornitina, citrulina y homocisteína (participan en el metabolismo de los aminoácidos - ciclo de la urea);
hidroxiprolina e hidroxilisina (forman parte de la composición del colágeno y algunas proteínas);
la sarcosina (o metilglicina).
Algunos aminoácidos también pueden tener importancia comercial o farmacológica.
- El glutamato de sodio se utiliza en la industria alimentaria como potenciador del sabor (ver cubo de caldo).
- La L-dihidroxifenilalanina (L-DOPA) es un medicamento que se usa para el tratamiento de la enfermedad de Parkinson.
- El 5-hidroxitriptófano (5-HTP) se ha utilizado para tratar los síntomas neurológicos asociados con la fenilcetonuria (una enfermedad metabólica hereditaria que impide el uso de fenilalanina, un aminoácido esencial, debido a deficiencias enzimáticas particulares; la acumulación de fenilalanina en los tejidos es responsable para lesiones cutáneas y neurológicas graves).
Las plantas y las bacterias son capaces de producir aminoácidos particulares, que se pueden encontrar en antibióticos peptídicos, como la nisina y la alameticina.
Aminoácidos esenciales
Algunos de los 20 aminoácidos ordinarios se denominan esenciales, ya que el cuerpo no puede sintetizarlos a partir de otros compuestos, sino que deben tomarse con los alimentos.
Para los seres humanos, estos son fenilalanina, leucina, isoleucina, lisina, metionina, treonina, triptófano, valina y, en los niños, histidina y arginina.
Aminoácidos ordinarios, características químicas.
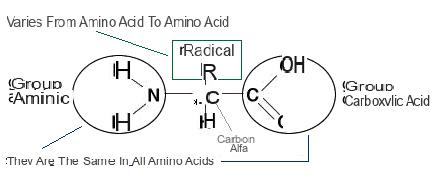
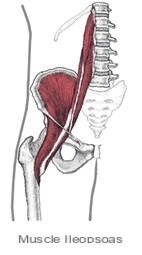
En función de las características químicas del radical R (grupo de átomos que forman una cadena no muy larga), los aminoácidos se pueden dividir en varias categorías.
Aminoácidos con R apolar (no capaces de formar enlaces de hidrógeno):
con catena alifatica: alanina, leucina, isoleucina, valina, prolina
con cadena aromática: fenilalanina, triptófano
con una cadena que contiene un átomo de azufre: metionina
Aminoácidos con R polar:
con gruppo OH: serina, treonina, tirosina
con grupo SH: cisteína
con grupo CO-NH2: asparagina, glutamina
con H: glicina (el único aminoácido no quiral)
Aminoácidos con R básico:
lisina, arginina, istidina
Aminoácidos con ácido R:
acido glutammico, acido aspartico